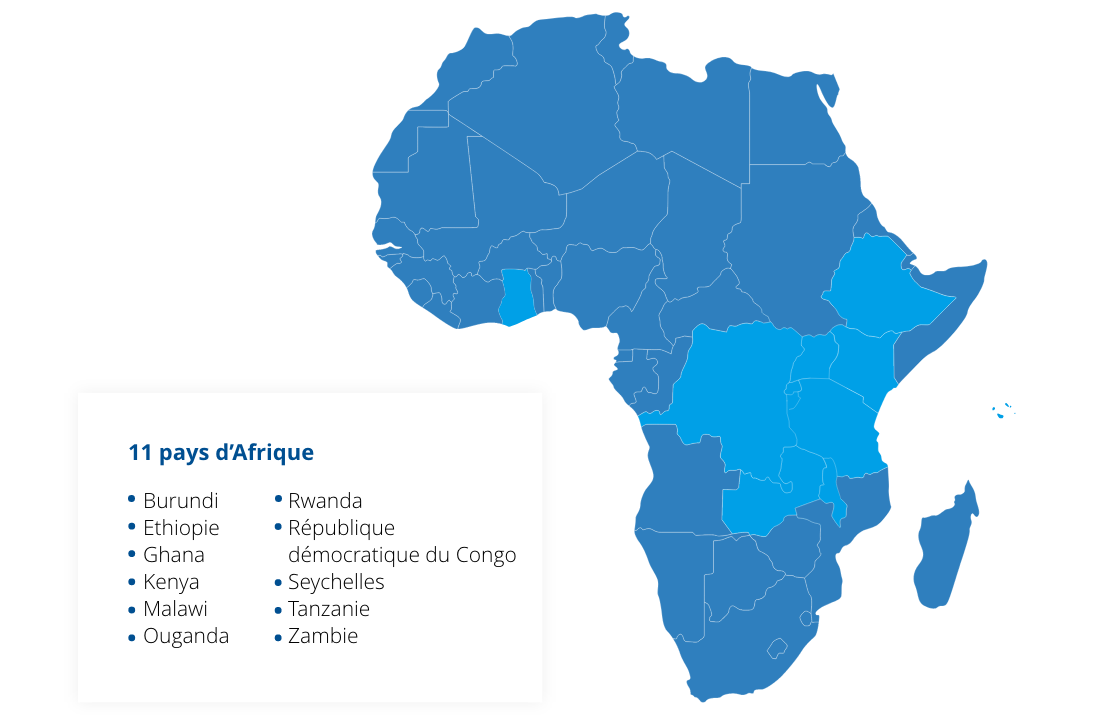
MEDISAFE est un projet visant à lutter contre les médicaments falsifiés dans 11 pays en Afrique de l’Est et du Centre : Burundi, Éthiopie, Ghana, Kenya, Malawi, Ouganda, République Démocratique du Congo, Rwanda, Seychelles, Tanzanie et Zambie. Il a été initié par l’Union européenne dans le cadre de l’Initiative des Centres d’Excellence pour la réduction des risques nucléaires, radiologiques, biologiques et chimiques (NRBC). Tous les pays participants sont des états membres du secrétariat régional de l’Initiative des Centres d’Excellence pour la zone Afrique de l’Est et du Centre.

La Commission européenne a sélectionné Expertise France pour mettre en œuvre le projet à la tête d’un consortium de 5 partenaires : APRO-PHISP (Association professionnelle des pharmaciens inspecteurs de santé publique), ASST Fatebenefratelli Sacco (Association de quatre CHU de la région Lombardie), CHMP (Centre humanitaire des métiers de la pharmacie), CIOPF (Conférence Internationale de l’Ordre des Pharmaciens Francophones) et REMED (Réseau Médicament et Développement).
Le comité consultatif se compose de l’OMS, de l’OCLAESP (Office central de lutte contre les atteintes à l’environnement et à la santé publique) et du RIVM (Institut national néerlandais de la santé publique et de l’environnement).
La stratégie du consortium consiste à apporter une réponse holistique à la problématique en se basant sur les recommandations de l’OMS et en capitalisant sur les projets déjà mis en place dans la région, notamment dans le cadre des Centres d’Excellence NRBC, dont l’un des objectifs est de soutenir la lutte contre la production et le trafic de médicaments falsifiés.
Les pays d’Afrique de l’Est et du Centre sont parfaitement conscients du problème. La Communauté de l’Afrique de l’Est (EAC) et un certain nombre de partenaires ont développé des activités en réponse à cette préoccupation à la fois au niveau national et en collaboration avec des organisations internationales, notamment Interpol, par exemple dans le cadre de l’opération Mamba, qui a abouti à la signature de la Déclaration de Zanzibar en 2010. L’Union africaine (UA) travaille à la création d’une Agence africaine des médicaments (AMA) qui contribuera à instaurer un environnement favorable au développement de l’industrie pharmaceutique, et permettra une meilleure coordination entre les différents partenaires et acteurs entreprenant des efforts pour renforcer et harmoniser la réglementation pharmaceutique sur le continent. L’AMA s’appuiera sur les structures déjà existantes à l’image de l’AMRH (Programme africain d’harmonisation des réglementations en matière de médicaments). Des initiatives pénales sont déjà en cours, comme le développement d’une loi modèle soutenue par le NEPAD (Nouveau Partenariat pour le développement de l’Afrique).
Les Centres d’Excellence NRBC sont pensés pour encourager la coopération et la coordination entre tous les niveaux de gouvernement et les partenaires internationaux afin de lutter contre les risques NRBC (Nucléaires, Radiologiques, Biologiques et Chimiques), qu’ils soient de nature criminelle, accidentelle ou naturelle. Cette initiative constitue une approche complète et cohérente couvrant la prévention des risques NRBC – préparation, réponse et réhabilitation – comprenant notamment les aspects juridiques, réglementaires, policiers, organisationnels et techniques. Elle est dirigée, financée et mise en œuvre par la Commission européenne, en étroite coordination avec le Service européen pour l’action extérieure (SEAE), avec le soutien de l’ONU (UNICRI), du Centre commun de recherche de la Commission et d’autres organisations internationales, ainsi que des experts locaux.